专家解读 | CHO重组表达产品上市申报前遗传稳定性研究要求
2024/12/18

遗传毒性杂质实践案例分享
微谱杂质研究中心
技术总监 李美玲

简介:李美玲,致力于药品在整个生命周期内各种创新药和仿制药的CMC药物质量研究,拥有近30个中美双报项目经验,包括各品种的分析方法的开发验证,注册资料撰写等,多次参与中国药监机构和美国检察官的项目交流和现场核查。此外,在质量研究尤其基因毒性杂质研究方面有着独特的经验和技巧,能够为客户提供定制化的杂质研究申报资料。

我们先看第一部分,杂质研究。从监管方来讲,肯定要按照法规要求,申报明确写出了是注册资料的哪一部分,必须做好审查监管;作为药品申报方来看的话,必须参照此标准做研究才能申报成功;从社会民生问题来讲,基因毒作用于人的DNA当中,关乎到下一代或者后代的发展,所以遗传物的改变被监管机构作为了特殊的物质,表明了一定要做详细研究。
我们知道在ICHQ里面,整个指导原则分三个大的部分,还有一个M系列。所以,我们基于杂质对药品质量的显著影响,无论进行任何药品都要进行杂质分析研究控制,目前对于公认的结构和致癌物提出了亚硝胺化合物、黄曲霉素、烷基、氧化偶氮基化合物等,有些结构基团被识别为具有较高的致癌性,即使摄入低于TTC水平,从理论上是有可能会导致癌症风险的。
站在挑战性来讲,我相信做杂质研究,都是遇到过很多扎心的事儿。比如说,供应路线从哪里评估?评估哪些?怎么分类?我的分析方法进一步怎么弄?如果超标了又么办?

我们先看第一部分,杂质研究。从监管方来讲,肯定要按照法规要求,申报明确写出了是注册资料的哪一部分,必须做好审查监管;作为药品申报方来看的话,必须参照此标准做研究才能申报成功;从社会民生问题来讲,基因毒作用于人的DNA当中,关乎到下一代或者后代的发展,所以遗传物的改变被监管机构作为了特殊的物质,表明了一定要做详细研究。
我们知道在ICHQ里面,整个指导原则分三个大的部分,还有一个M系列。所以,我们基于杂质对药品质量的显著影响,无论进行任何药品都要进行杂质分析研究控制,目前对于公认的结构和致癌物提出了亚硝胺化合物、黄曲霉素、烷基、氧化偶氮基化合物等,有些结构基团被识别为具有较高的致癌性,即使摄入低于TTC水平,从理论上是有可能会导致癌症风险的。
站在挑战性来讲,我相信做杂质研究,都是遇到过很多扎心的事儿。比如说,供应路线从哪里评估?评估哪些?怎么分类?我的分析方法进一步怎么弄?如果超标了又么办?

我们看一下流程:首先是工艺评估,然后到毒理评估,再到毒理定限度,最后再制定分析方法,让方法建立后进行方法验证,再进行控制策略。
我们从一开始工艺怎么进行评估呢?我们要知道来源是什么,我们要知其然,知其所以然。所以,很多时候企业找到我,问我做过这些杂质吗?我做过不代表您产品的情况,包括他家用盐酸,你家用硫酸,就可能会产生不同的东西。基于他们来源,来自于哪里,我们就进行怎么样的控制,比如说原料生产工艺、工艺控制等等。
关于毒理,我们按照ICHM7专家规则和统计学规则、两个规则等得出一个定性的情况。我在这里想说的是,所有软件、规则都是基于工具,最终评判还需要毒理专家,如涉及一个规则是阳性,一个规则是阴性,这时候如何定性,这需要毒理专家基于背后逻辑去反复评估,最终得出一个准确的定性结果。
做毒理评估是基于某种目标物去进行评估的,给你一个目标物,它可能没有PDE值,我们的评判是不能脱离品种的,我们的控制是不脱离品种的。所以,基于品种暴露情况和特性最终定一个安全的阈值,这是非常重要的。

刚才韩老师讲了“定性”的情况,这里我希望把定性和定量整体串一下。这里有一个案例,我选择了相关分析的参数,甚至经过最后的优化建立了该方法的合适条件,大家可以看到降解产物。对这些降解产物来讲,后续如何进行定性,这里给出了对于杂质IM001-IM005进行了LCMS、LCMSMS,SC-Q-TOF杂质结构推导。
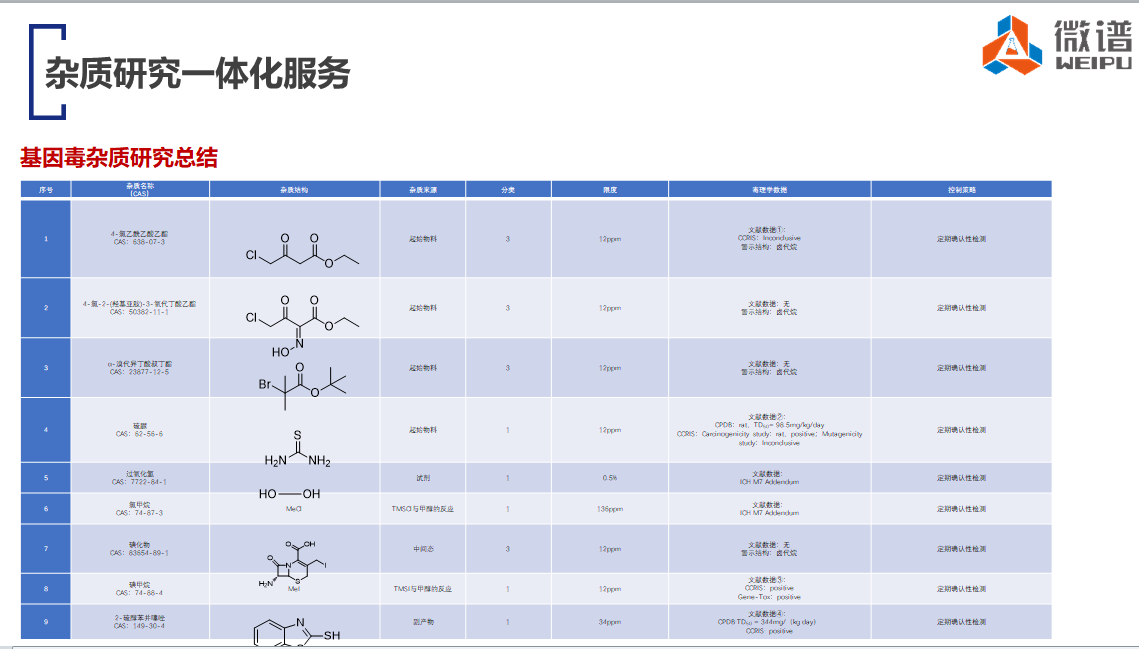
最后,到了分析环节。基因毒杂质一般就有高反应性和基质效应,这时候我们该怎么做呢?包括它的一些特殊性,包括我们从正确的理解来看是不存在这种情况的,但是有检出,这时候要从整个实验环境来分析,基因毒的分析对实验室要求是很高的,是按照BSL2级去设计实验的。有些时候,你们的分析环境达不到要求,所以才会存在家阳性的情况。不管是进空气,进空白都无法排除干扰,都会造成一系列的问题,因为活性非常强,整体来讲就会存在这种问题。
比如有家企业找过我们,我们帮他们做了一系列分析,排除其他家的检出情况,这些不仅仅是实验问题,也存在着环境问题。
基于前面的这些情况,我们要对生产环境有不同的理解和认知,通过不同方法和维度理解杂质。我们分几个维度:第一,根据路线长短情况。比如说,物质的来源、去向在哪里,我们要明确清楚。在原料标准中包含对杂质的检测,根据ICHQ6A进行定期检测。第二,对API的来源清楚,但对去向不清楚的时候,这就要采用不同手段来判断物质的存在情况。第三,物质具体我们API很近,这时候需要根据来源情况去做相应的方法。第四,有些东西是存在降解产物,在这里要特别提醒一下:如果是降解产物要特别注重,这时候整个方法要进行考虑。我们碰到过很多种情况,他可能委托别家做了开发验证,但是开发验证做的不够充分,也报上去了,当药监局让他启动后续时,这家企业方法不能重现,这时候很要命,你去替换方法很麻烦,就会委托我们来确定方法,我们明显会看到方法是有缺陷的。
刚才韩老师讲了“定性”的情况,这里我希望把定性和定量整体串一下。这里有一个案例,我选择了相关分析的参数,甚至经过最后的优化建立了该方法的合适条件,大家可以看到降解产物。对这些降解产物来讲,后续如何进行定性,这里给出了对于杂质IM001-IM005进行了LCMS、LCMSMS,SC-Q-TOF杂质结构推导。

我们简单总结一下。前面跟大家说了做基因毒性杂质,要从工艺、毒理、分析三个模块,所以我们需要工艺团队、毒理团队和分析团队,共同协同合作完成这件事情。在能力要求上,我们需要产品的相关信息、毒理知识、分析方法的开发验证能力、数据库情况(强大数据库)、注册相关的申报策略等。面临仅有一次的发补机会,前期还需要做到充分识别,科学研究,否则面临发补会很焦虑。