专家解读 | CHO重组表达产品上市申报前遗传稳定性研究要求
2024/12/18

2021年2月19日,君实生物宣布,其自主研发的抗PD-1单抗药物特瑞普利单抗注射液(拓益®)获得国家药品监督管理局NMPA批准,用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌(NPC)患者的治疗,成为全球首个获批鼻咽癌治疗的抗PD-1单抗,实现了该领域内免疫治疗零的突破。
资料来源:https://mp.weixin.qq.com/s/1fDbLu_aV3K3HsvUFA_eeQ
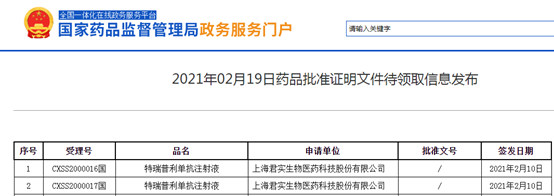
来源:国家药品监督管理局网站
公开资料显示,截至目前,特瑞普利单抗已在黏膜黑色素瘤、鼻咽癌、软组织肉瘤领域获得FDA授予1项突破性疗法认定,1项快速通道资格和3项孤儿药资格。特瑞普利单抗(拓益®)也是首个获得FDA突破性疗法认定的国产抗PD-1单抗。2020年12月,特瑞普利单抗成功通过中国国家医保谈判,被纳入新版目录。
作为全球首个获批的鼻咽癌免疫治疗单抗药物,微谱很荣幸也参与其中,2017年对其进行相容性等业务板块的支持,此次 [特瑞普利单抗注射液] 获批上市,是继黑色素瘤之后,特瑞普利单抗(拓益®)在国内获批的第二个适应症,也将为中国鼻咽癌患者带来创新的治疗方案和更长的生存获益。
在92例接受过至少二线系统化疗失败的复发/转移性鼻咽癌患者中,特瑞普利单抗单药治疗的客观缓解率(ORR)为23.9%,中位缓解持续时间(mDOR)达到14.9个月,疾病控制率(DCR)为41.3%,中位总生存时间(mOS)达到15.1个月。