专家解读 | CHO重组表达产品上市申报前遗传稳定性研究要求
2024/12/18

关于公开征求《治疗用重组蛋白药物上市许可申请质量综述资料撰写指导原则(征求意见稿)》等三个指导原则意见的通知
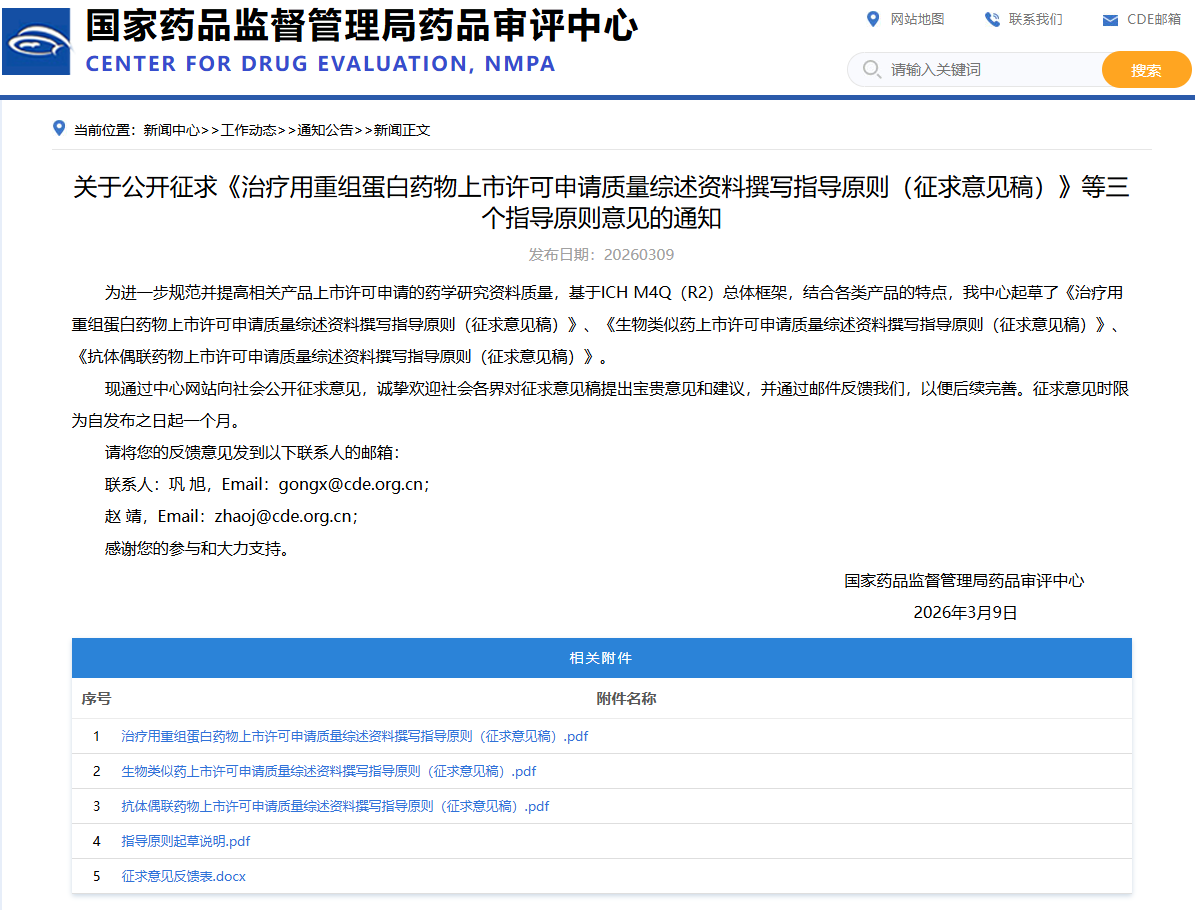
▲ 图源 | CDE官网
为进一步规范并提高相关产品上市许可申请的药学研究资料质量,基于ICH M4Q(R2)总体框架,结合各类产品的特点,我中心起草了《治疗用重组蛋白药物上市许可申请质量综述资料撰写指导原则(征求意见稿)》、《生物类似药上市许可申请质量综述资料撰写指导原则(征求意见稿)》、《抗体偶联药物上市许可申请质量综述资料撰写指导原则(征求意见稿)》。
现通过中心网站向社会公开征求意见,诚挚欢迎社会各界对征求意见稿提出宝贵意见和建议,并通过邮件反馈我们,以便后续完善。征求意见时限为自发布之日起一个月。
请将您的反馈意见发到以下联系人的邮箱:
联系人:巩 旭,Email:gongx@cde.org.cn;
赵 靖,Email:zhaoj@cde.org.cn;
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2026年3月9日
扫描二维码,查看附件

更多详情 · 请联系
电话:021-3178-5055
邮箱:yiyao-marketing@weipugroup.com