专家解读 | CHO重组表达产品上市申报前遗传稳定性研究要求
2024/12/18

精彩呈现:遗传毒性杂质研究实践案例分享
李美玲老师表示药学分析服务部作为专业的一体化分析测试平台,涵盖药品研制各阶段的分析需求,精准助力药品国内外申报。从研发到生产,从原料药到制剂,从IND到NDA,微谱会快速并准确的为客户提供评估报告、方法开发验证报告和分析测试结果。

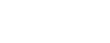
目前“杂质谱”遗传毒性杂质研究与控制的思路与策略发生了深刻变化,由“以终为始”战略转移为“以源为始”,基于科学和风险的药品控制理念,制定从工艺化学到毒理学、分析化学,最后制定控制策略的完整研究流程。

三大案例 为您重点解读
为了让大家更加直观清晰的理解工艺评估、毒理评估、分析方法的原理,李美玲老师特别分享了具体案例,涵盖从研究流程、可能存在的误区、决策逻辑等进行全方位解析。
案例一 【工艺评估】解读

在工艺评估阶段,通过工艺流程得到基因杂质清单,李美玲老师着重强调了四个误区:
误区1:所有的同分异构体都是基因毒
解析:苯胺上邻位二取代,不作为警示结构,不作为基因毒性杂质。
误区2:所有识别出来的基因毒都直接开方法做验证
解析:起始物料中检测,根据结果判断是否需要进行相对应的氯酰胺化合物的研究,可根据起始物料的研究结果,进行选择性研究。
误区3:错把溶剂残留当基因毒控制
解析:无警示结构,可在溶剂残留中控制。
误区4:胺类试剂的使用遗漏N-亚硝胺化合物
解析:二乙胺中杂质一乙胺与中间体反应,酸性条件下,该杂质与残留试剂亚硝酸钠,反应得到N-亚硝胺化合物。
李美玲老师用实验图谱加数据的方式一一解读,一层层的推理讲解将现场的讨论推向高潮。
案例二 【毒理评估】解读
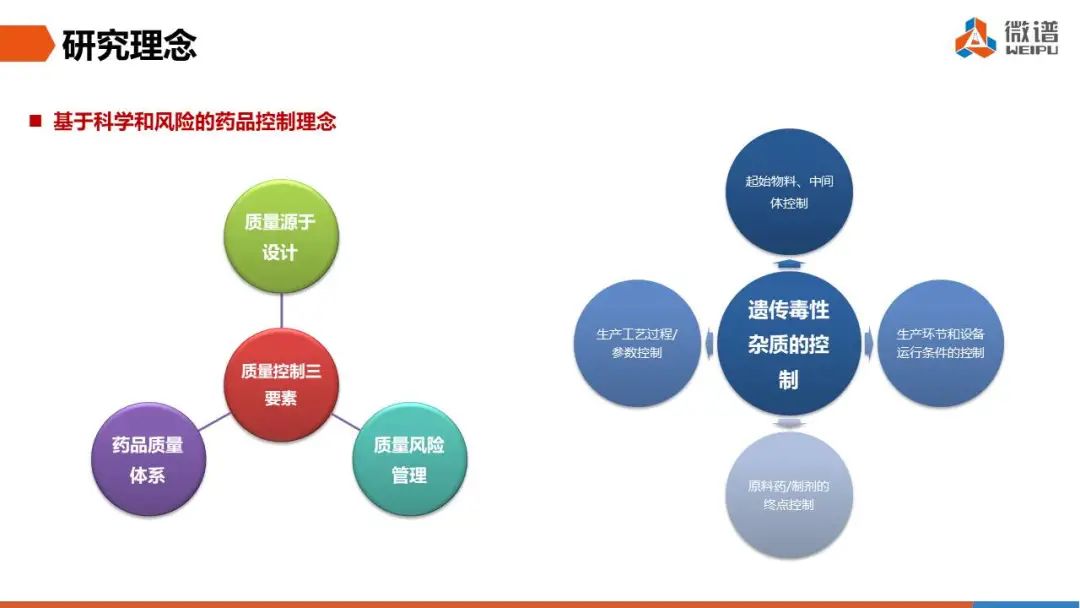
在毒理评估阶段,从毒理评估决策逻辑、不同途径的选择、相似物的选择等方面进行全面解析。

毒理评估时,需要有明确的毒理评估决策逻辑,不同的给药途径需要判断数据是否重组进行毒理学风险评估。相似物的选择以脂肪胺为例,需要具有一定相似度的物质进行评价,相似度90%以上的物质有几百个,参考REACH评估与OECD指导原则,决定使用相似度92%的三丁胺评估,最后获得FDA510K批准。
案例三 【分析方法】解读

在分析方法建立阶段,以羟胺为例,分子量只有33,理化特征小,依照药典的前处理3步衍生复杂,不满足ppm级别的灵敏度,经过Scan全扫,无论是正离子模式还是负离子模式得到的都是无信号结果。因此微谱通过衍生试剂选择环己酮、碱性条件选择0.1%氨水、反应温度45℃、反应10分钟、1.5N当量环己酮,最终得到了漂亮的MS图和完美的PDA图。
不过同样的羟胺,不同的药品基质衍生化条件不同,需要结合药品的特性选择、调整不同的方法,以满足不同的ppm级别、不同药品基质的灵敏度、准确度等验证指标。


综上,杂质研究需要工艺团队、毒理团队、分析团队的协同合作,结合产品相关信息、工艺化学知识、毒理知识、方法开发与验证知识及能力、强大的数据库和注册相关的申报策略,最终满足客户的需求。